С.І. Жук, д.м.н., професор кафедри акушерства, гінекології і перинатології НМАПО ім. П.Л. Шупика
Н.П. Дзісь к.м.н., кафедра акушерства і гінекології № 2 Вінницького національного медичного університету ім. М.І. Пирогова
Однією з основних скарг при зверненні жінок до лікаря акушера-гінеколога є біль. Так, за даними ВОЗ, кожна п’ята жінка у світі страждає від болю (Подзолкова Н.М., 2003). Однак після проведеного складного та дорогого обстеження пацієнтки не завжди підтверджується гінекологічне походження болю. Виявити анатомічні (органічні) зміни в органах малого тазу найчастіше не вдається. Тому таких жінок консультують спеціалісти багатьох спеціальностей: урологи, невропатологи, психіатри, проте лікування, яке вони призначають, на жаль, не приносить полегшення. Хворі на хронічний сальпінгоофорит становлять основну групу пацієнток, які звертаються до жіночої консультації з цього приводу. Це обумовлює встановлення таких діагнозів, як хронічний аднексит, аднексит у стадії загострення, підгострий сальпінгоофорит. Чи завжди є обгрунтованим зазначений діагноз, особливо коли жінка скаржиться лише на біль без інших ознак запалення? Зважаючи на це, чи є доцільним призначення протизапальних препаратів, особливо у вигляді антибактеріальної терапії?
Інколи жінки не лише не відчувають полегшення страждання, а в них ще навпаки погіршується стан здоров’я (дисбактеріози, алергічні прояви тощо).
У зв’язку з вищезазначеним ми звернулися до Міжнародної класифікації хвороб 10-го перегляду (МКХ-10), зокрема хвороб жіночої статевої сфери.
Один із розділів «Незапальні хвороби жіночих статевих органів» (НХВСО) (N80 – N98) виглядає таким чином:
N80 – ендометріоз;
N83 – незапальні ураження яєчника, маткової труби та широкої зв’язки матки;
N83.0 – фолікулярна кіста яєчника;
N83.1 – кіста жовтого тіла;
N83.2 – інші та неуточнені кісти яєчника; виключено кісти, пов’язані з аномаліями розвитку; неопластична; синдром полікістозних яєчників;
N83.3 – набута атрофія яєчника і маткової труби;
N83.9 – незапальні ураження яєчника, маткової труби та широкої зв’язки матки; неуточнені ураження;
N85 – інші незапальні ураження матки, за винятком шийки матки;
N85.0 – залозиста гіперплазія ендометрія;
N85.1 – аденоматозна гіперплазія ендометрія;
N87 – дисплазія шийки матки;
N91 – відсутня, мізерна та нечаста менструація;
N92 – надмірні, часті та нерегулярні менструації;
N92.6 – інша неуточнена нерегулярна менструація;
N94 – біль та інші стани, пов’язані з жіночими статевими органами і менструальним циклом;
N94.0 – міжменструальний біль;
N94.3 – синдром передменструального напруження;
N94.4 – первинна дисменорея;
N94.5 – вторинна дисменорея;
N 94.6 – неуточнена дисменорея;
N 94.9 – стани, пов’язані з жіночими статевими органами і циклом; неуточнені стани;
N96 – звичайний викидень;
N97 – жіноча безплідність.
Проаналізувавши захворювання, які входять до цього розділу, можна зробити висновок, що загальним патогенетичним механізмом є дисгормональні порушення різного рівня. Основним симптомом при цьому може бути хронічний тазовий біль.
Хронічному тазовому болю присвячено чимало публікацій. Основна мета лікаря при такому стані – визначення причин походження болю (органічний чи функціональний). Відчуття болю може бути однаковим при хронічному аднекситі, ендометріозі та інших незапальних захворюваннях внутрішніх статевих органів, тому-то першочергово при аналізі НХВСО ми розглядаємо дисгормональні порушення.
Прояви дисгормональних порушень можуть бути різними (недостатність лютеїнової фази, персистенція жовтого тіла, синдром лютеїнізації фолікула, в якому не відбулась овуляція, синдром ановуляції – персистенція фолікула, атрезія фолікула, синдроми гіпогонадизму гіпофізарного чи гіпоталамічного). В основі дисгормональних порушень лежить абсолютна чи відносна недостатність статевих гормонів або порушення їхнього кількісного співвідношення. Маніфестація дисгормональних порушень найчастіше відбувається в активному репродуктивному віці, однак розвиваються вони без вираженої клінічної картини задовго до цього – в період статевого розвитку підлітків. Період статевого розвитку та пременопауза є критичними віковими періодами (Подзолкова Н.М., 2003). Спочатку ці порушення носять функціональний характер, а згодом вони формують патологічні «замкнуті кола» різних патофізіологічних станів, які визначаються як «незапальна хвороба внутрішніх статевих органів».
Захворювання – це насамперед порушення системи саморегуляції та зворотної аферентації, тобто порушення двобічного зв’язку між центральною нервовою системою та периферичними органами.
Існує думка, що репродуктивна система жінок є найуразливішою, оскільки основний принцип її функціонування полягає у саморегуляції та аферентації (позитивний і негативний зворотний зв’язок).
Перехід компенсаторно-пристосувальних реакцій у хворобу зазвичай відбувається при спадковій схильності, а також при нейрообмінних порушеннях (надлишкова чи недостатня вага і т.ін.). Гіпоталамус, гіпофіз та яєчник – основні механізми у складному біологічному годиннику жінки. Найчастіше зміни відбуваються в нервовій системі (порушення обміну серотоніну, дофаміну, опіатів тощо), що призводить до порушення обміну пролактину та інших гормонів. Повноцінність будь-якої фази менструального циклу (МЦ) завжди визначається попередніми МЦ, з урахуванням циклу негормонально- та гормональнозалежної фаз росту фолікула. Найчастіше відносна або абсолютна недостатність чи надлишок естрогенів у першу фазу циклу і є причиною дисгормональних порушень як мінімум в трьох МЦ. Естрогени також необхідні для синтезу рецепторів до прогестерону і для збільшення рівня простагландинів.
При наступних один за одним МЦ формується стійка дисфункція яєчників. У яєчниках накопичується тека тканини атретичних фолікулів, кількість яких з кожним неповноцінним МЦ збільшується; більш тривале існування тканини жовтого тіла призводить до формування полікістозних яєчників або функціональних кіст. В ендометрії внаслідок ендокринних порушень формується неповноцінність секреторної фази, атрофічні та гіперпластичні процеси. Всі ці стани є проявом НХВСО.
При тривалому патологічному процесі з часом відбувається зміна домінуючого чинника патогенезу, і в зв’язку з цим може змінюватися клінічна картина. Саме тому надзвичайно важко визначити справжню причину захворювання. У такому разі ці захворювання класифікуються відповідно до МКХ-10 як неуточнені.
Виникнення відчуття болю при цьому можна трактувати як наслідок дисгормональних порушень, оскільки тривалий дисбаланс стероїдних гормонів призводить до дисбалансу простагландинів F2α та E2, що і є основною причиною болю.
Проаналізувавши дані літератури, присвячені проблемі хронічного тазового болю, можна зробити висновок, що біль може виникати: за наявності запалення в даний час; після гострого запалення, що мало місце багато років назад; а також без запалення.
Немає потреби перераховувати всі патологічні стани, однак варто звернути увагу на біль, що виникає після запалення (гострого запалення, що було багато років тому). Це важливо, оскільки сьогодні гіподіагностика НХВСО лежить в основі немотивованого призначення багаторазових курсів медикаментозної терапії та хірургічного втручання, об’єм яких з кожним разом збільшується.
Згідно з етіологічним підходом, хронічний тазовий біль, що триває понад 6 міс, найчастіше супроводжується змінами психіки та поведінки жінок. Таким чином, спрощуючи складні механізми виникнення болю, можна стверджувати, що йому властиві центральні та периферичні механізми походження. До важливих слід віднести дегенеративно-дистрофічні зміни рецепторного та провідних шляхів периферичної нервової системи, зміни в обміні серотоніну, дофаміну, опіатів, а також порушення кровообігу на різних рівнях (органному, тканинному). Тривалий перебіг патологічного стану обумовлює дегенерацію рецепторного апарату тазових органів і дистрофії клітин.
Такі ж процеси можуть відбуватися, коли запалення в органі було багато років тому, але особливості реактивності організму (що передаються спадково), особливості психічного статусу формують біль за принципом «фантомного». Цей термін пропонується для трактування больового синдрому при НХВСО, коли в анамнезі пацієнтка хворіла на гострий аднексит, а на даний час діагноз хронічного аднекситу та інших НХВСО, наприклад ендометріозу, виключено. Отже, в першу чергу в даному випадку причинами болю є зміни в рецепторному апараті, які виникли протягом багатьох років після дії подразника (збудників захворювання, медіаторів запалення та ін.). У такому разі за браком ознак хронічного запалення (відсутність збудника, лабораторних ознак, змін за результатами УЗД та ін.) встановлюється діагноз НХВСО. Але чим триваліший час від початку ймовірної дії подразника, тим стійкішими є зміни в нервовій системі.
Інший варіант виникнення болю – коли в анамнезі у жінки не існує даних щодо гострого чи запального процесу, а також виключено ендометріоз, тобто діагноз НХВСО неясного генезу. Що може спричинити виникнення тазового болю у такому разі? На нашу думку, – це дисгормональні зміни, які призвели до порушення мікроциркуляції на тканинному рівні з відповідним утворенням метаболітів, характерних для ішемії (перекиси та інші окисли). А хронічна гіпоксія обумовлює дистрофічні зміни в рецепторному апараті жіночої статевої сфери.
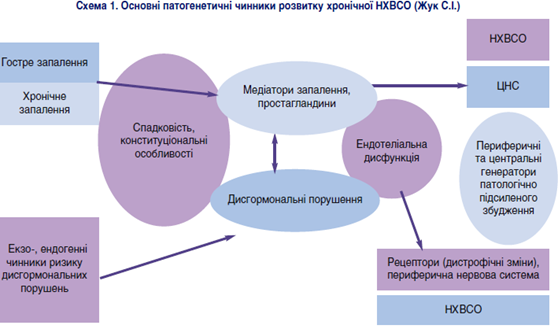
Таким чином, підсумовуючи ймовірні механізми виникнення болю, можна стверджувати, що їхньою причиною є дисгормональні порушення, порушення синтезу нейромедіаторів, опіатів, мікроциркуляції (ендотеліальна дисфункція) (схема 1). На нашу думку, ендотеліальна дисфункція є найуразливішою та найбільш чутливою в патогенезі виникнення хронічного тазового болю при НХВСО, оскільки судини в першу чергу реагують на зміни рівня гормонів.
При стійкому порушенні мікроциркуляції в зоні ішемії утворюються активні метаболіти, що модифікують зворотний зв’язок із центральними відділами регуляції. Формуються так звані периферичні та центральні генератори патологічно підсиленого збудження (Крижанівський Г.Н., 1980, 1995).
Важливим чинником у виникненні болю є також антиноцицептивна система (протибольова). Ноцицептивна та антиноцицептивна системи мають складні біохімічні складові, але їх поєднують особливості обміну нейромедіаторів, особливо серотоніну.
При недостатній кількості серотоніну виникає біль.
Слід зауважити, що це спрощений погляд на дану проблему, який потребує окремого розгляду в наших публікаціях надалі.
Таким чином, однією з основних причин НХВСО є дисгормональні порушення та порушення мікроциркуляції, що формують основні патогенетичні ланцюги.
Проведені нами дослідження рівня гонадотропних та статевих гормонів у жінок з НХВСО також вказують на наявність нейроендокринних порушень, що потребують подальшого вивчення та відповідної корекції.
На нашу думку, розглядаючи проблему незапальної хвороби придатків матки в контексті цілісного організму та вивчаючи патогенетичні механізми її розвитку, також доцільним було б визначення стану ендотелію судин, оскільки виникнення його дисфункції лежить в основі розвитку найбільш розповсюджених соматичних захворювань, характерною рисою яких вважають порушення мікроциркуляції, зміни процесів ангіогенезу та утворення вазоактивних речовин.
Ендотелій, як відомо, є основним функціональним компонентом судинної стінки, який відіграє важливу роль у підтримці тонусу та структури судин, локального гомеостазу, забезпечує ряд біологічно активних процесів в організмі, динамічну рівновагу між вазодилатуючими та вазоконстрикторними чинниками, регулює ріст та проліферацію субендотеліальних клітинних та позаклітинних структур, а також впливає на проникність судин.
Тому на особливу увагу заслуговує вивчення ендотеліальної дисфункції як незалежного чинника ризику незапальної хвороби придатків матки. У числі основних причин, що призводять до виникнення такого патологічного стану, лежать також зміни процесів ангіогенезу і утворення вазоактивних речовин. При дослідженнях рівня маркерів дисфункції ендотелію простацикліну та ендотеліну-1 при НХВСО виявлено зменшення концентрації простацикліну та підвищення рівня ендотеліну-1, що може бути наслідком спазму судин як локально, так системно, і з часом спричиняти розвиток дисфункції ендотелію. Результати дослідження вказують на те, що при НХВСО виявляється дисфункція ендотелію, що потребує подальших досліджень для визначення патогенетичних ланок та критеріїв діагностики цього патологічного стану.
Як додатковий метод дослідження для вдосконалення діагностики незапальної хвороби придатків матки ми проводили ехографічне обстеження органів малого тазу з використанням ультразвукової доплерометрії для визначення показників швидкості кровотоку в різних відділах судинного русла. У результаті ехографічногообстеження виявлено гіпоплазію матки, невідповідність товщини ендометрія фазам МЦ та кістозні зміни в яєчниках. Доплерометрично для НХВСО характерне підвищення числових значень індексів опору в маткових, яєчникових артеріях і гілках маткових артерій, що супроводжується сповільненням швидкості кровотоку, порушенням кровозабезпечення внутрішніх статевих органів (Жук С.І., Дзісь Н.П., 2007).
Таким чином, у розпочатих дослідженнях підтверджено той факт, що ендотеліальна дисфункція є однією з головних причин розвитку НХВСО.
Також нами вивчено функціональний стан гіпоталамогіпофізарно-яєчникової системи у жінок, які страждають на НХВСО. Було доведено, що у пацієнток із НХВСО органів наявне порушення нейроендокринної регуляції (гіпофізарної ланки регуляції стероїдогенезу та гормональної функції яєчників).
Слід зауважити, що при формуванні груп хворих на НХВСО, з використанням ендоскопічних методик ми завжди проводили диференційний діагноз з ендометріозом та іншими захворюваннями, котрі не відносяться до НХВСО. Проведений аналіз анатомофункціонального стану репродуктивних органів у пацієнток з незапальною хворобою придатків матки свідчить, що застосування ендоскопічного методу обстеження дає змогу не тільки верифікувати патологію органів малого тазу, визначати об’єм та метод хірургічного лікування, але й утриматися від необгрунтованих оперативних утручань, надаючи перевагу тим чи іншим консервативним методам залежно від патологічного стану.
Стосовно лікувальних заходів варто зазначити, що визначення НХВСО сприяє скороченню до мінімуму застосування великої кількості фармакологічних засобів, виключаючи неефективні. Це дозволить зменшити фармакологічне навантаження на організм і відповідно – кількість побічних дій препаратів, а також заощадити грошові кошти пацієнток.
Загальновідомо та підтверджено практикою, що основні виражені дисгормональні порушення закладаються в дитячому та підлітковому віці (альгодисменорея та інші порушення овуляційно-менструального циклу). У зв’язку з цим особливу увагу слід надавати перебігу даного періоду життя: психічним особливостям дівчаток (тривожні стани, схильність до депресії), фізичному, розумовому напруженню. За даними літератури, стан нервового перенапруження значною мірою визначається функціональною асиметрією півкуль головного мозку. Лабільність функціонального стану півкуль головного мозку посилює кортикогіпоталамічні і лімбікоретикулярні співвідношення, за рахунок яких в основному і підтримується нервове перенапруження (Брагина И.Н.).
Існують праці, що вказують на те, що суїцидальні спроби у дівчаток-підлітків пов’язані з депресивними станами внаслідок порушення балансу стероїдних гормонів (гіпоестрогенемії), які достатньо успішно корегуються застосуванням гормональних препаратів. У зв’язку з цим прийом комбінованих оральних контрацептивів (КОК) (за умови регулярного статевого життя) буде, безумовно, патогенетичним.
Наявність великої кількості КОК (Ліндинет 20, Ліндинет 30, Новінет, Регулон) з різним вмістом етинілестрадіолу та різними прогестинами з відповідними індексами селективності дає змогу призначати їх індивідуально, особливо дівчаткам-підліткам. Так, у підлітковому віці (якщо застосування КОК можливе) слід призначати препарати з мінімальним вмістом гормонів як естрогенів, так і прогестинів.
Мінімальна кількість естрогенів (20 мкг) входить до складу Новінету та Ліндинету 20. Завдяки тому, що ці препарати містять різні прогестини з різними індексами селективності, це дає змогу підбирати їх індивідуально, в залежності від конституціонального типу, тобто з урахуванням можливої рецепторної взаємодії. Так, Новінет рекомендують призначати дівчаткам-підліткам та жінкам віком старше 35 років з ектоморфним (кістковим) конституціональним типом (перевага гестагенів та андрогенів), а Ліндинет 20 – при ендоморфному (жировому) конституціональному типі (перевага естрогенів). Пацієнткам репродуктивного віку (в 20-35 років), коли найчастіше спостерігаються періоди гормональних змін в організмі (МЦ, пологи, аборти, запальні хвороби та ін.), призначають КОК, до складу яких входить 20 мкг (Ліндинет 20 і Новінет) та 30 мкг етинілестрадіолу (Ліндинет 30 і Регулон) з різними прогестинами (дезогестрел та гестоден) і відповідними індексами селективності та спорідненості до прогестеронових рецепторів. Зокрема, Ліндинет 20 призначають жінкам ендоморфного (жирового) конституціонального типу, Регулон – мезоморфного (м’язового) конституціонального типу (перевага андрогенів), Новінет – ектоморфного (кісткового) конституціонального типу. Ліндінет 30 також рекомендується пацієнткам, яким не підходить Ліндинет 20, або тим, які перенесли запальні захворювання статевих органів (Жук С.І., Захурдаєва Л.Д., 2008; Овсяннікова Т.В., Арсіян А.Б., 2008).
Зазначений метод, упроваджений нами, дає можливість досягти швидкого клінічного ефекту, зменшити ймовірність побічних дій і забезпечити тривале застосування препаратів Новінет, Регулон та Ліндинет 20.
Існує позитивний досвід застосування Ліндинету 20, Ліндинету 30, Новінету та Регулону для усунення дисгормональних порушень за рахунок нормалізації рівнів гормонів. Ліндинет 20 рекомендуємо призначати при ендометріозі та альгодисменореї, нейроендокринному синдромі, дисгормональних захворюваннях молочних залоз; Ліндинет 30 – після запальних захворювань; Новінет – при лейоміомах матки; Регулон – при гіперпластичних процесах, порушеннях овуляторно-менструального циклу (гіперполіменореї), гіперандрогеніях різного генензу, склерокістозі яєчників, після абортів, апоплексії яєчників, при функціональних кістах та після оперативних утручань на органах малого тазу з профілактичною метою.
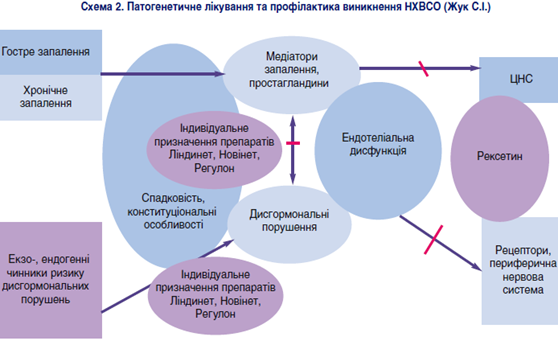
Враховуючи сказане вище, патогенетичним буде застосування КОК при НХВСО, особливо при ендометріозі (схема 2).
Окрім того, слід звернути увагу на застосування селективних інгібіторів зворотного захвату серотоніну (СІЗЗС), зокрема пароксетину, при незапальній хворобі. Вищенаведені дані щодо ролі серотоніну в патогенезі НХВСО, особливо в разі їхньої хронізації та перебігу з вираженою судинно-вегетативною симптоматикою, невротичними та тривожними станами, обгрунтовують призначення СІЗЗС – препарату Рексетин (виробництво компанії «Ріхтер Гедеон», Угорщина). Пароксетин серед відомих у практиці СІЗЗС має найбільш виражену анксіолітичну (протитривожну) дію, широко застосовується не лише в психоневрології, а й в кардіології, ревматології, гастроентерології та ін. На наш погляд, застосування пароксетину (Рексетину) в комплексному лікуванні незапальних патологій має широкі перспективи, потребує подальшого вивчення, детального аналізу та вироблення практичних рекомендацій. Розглядаючи цю групу препаратів для лікування НХВСО, є виправданим з позиції генезу формування та виникнення болю, оскільки СІЗЗС можуть впливати на центральний та периферичний ланцюги його розвитку. Також СІЗЗС усувають тривожні та депресивні стани, які утворюються вторинно, після формування хронічного тазового болю.
Однак доречним буде відмітити, що на етапі встановлення діагнозу НХВСО можуть маскуватися психіатричні та неврологічні захворювання (нейрогенні абдоміналгії), що потребують спеціалізованої допомоги. При нейрогенній абдоміналгії хронічний тазовий біль може бути основним симптомом депресії та тривожних станів, тобто психічні розлади є вторинними.
Таким чином, яким би складним не було визначення НХВСО, вибір правильного лікування має велике значення для пацієнтки і сприятиме покращанню якості життя жінки та збереженню її репродуктивного здоров’я.
Рубрика Инфекции, Статьи и публикации






Отзывов нет
Комментариев пока нет.
Оставьте свой отзыв