С.И. Жук, д.м.н., профессор кафедры акушерства, гинекологии и перинатологии НМАПО им. П.Л. Шупика
С.Н. Косьяненко, к.м.н., заведующая кабинетом гинекологической эндокринологии и маммологии;
В.А. Кулик, Центр матери и ребенка, г. Винница

Состояние молочных желез (МЖ) – один из самых чувствительных показателей нарушений в репродуктивной системе женщины. Как известно, заболевания гениталий тесно связаны с нарушениями в системе гипоталамус-гипофиз-яичники. Именно поэтому частота патологических изменений в МЖ при различных гинекологических заболеваниях достигает 80-92%. Группу наиболее высокого риска по развитию заболеваний МЖ как доброкачественного, так и злокачественного характера, составляют женщины с гиперпластическими процессами эндо- и миометрия (миома матки, эндометриоз, гиперплазия эндометрия).
При этом возрастной фактор не оказывает существенного влияния на степень проявления патологических процессов в МЖ.
Необходимо отметить, что доброкачественная дисплазия МЖ (ДДМЖ) является самым распространенным заболеванием МЖ. Ее частота в популяции составляет 40-65% и повышается в несколько раз при гинекологических заболеваниях [3, 8].
Согласно литературным данным, особенностью реакции МЖ при гиперпластических процессах гениталий является развитие пролиферативных форм мастопатии, обусловленное преобладанием гиперплазии железистой ткани по типу аденоза. Наиболее выраженные формы мастопатии с гиперплазией железистой ткани возникают у больных эндометриозом.
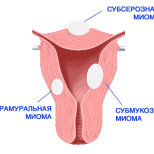
У женщин с миомой матки преобладает развитие фиброзной ткани в МЖ с тенденцией к формированию узловых форм заболевания.
При гиперандрогении наблюдаются фибрознокистозные изменения МЖ с ярко выраженным фиброзным компонентом. У пациенток с синдромом поликистозных яичников в МЖ чаще происходят гипопластические процессы с преобладанием жировой ткани, фиброзного компонента и реже отмечаются гиперпластические изменения [2, 7]. Доказано, что у женщин с гиперпролактинемией при высоком уровне пролактина в МЖ преобладают иволютивные процессы, вызванные центральными механизмами регуляции гонадотропинов и снижением функции яичников, что и проявляется гипоэстрогенией. При функциональной гиперпролактинемии частота жировой инволюции низкая, в МЖ преобладают гиперпластические процессы (аденоз).
При воспалительных процессах матки и придатков из-за длительных нарушений функции гипоталамояичниковой системы до 50% женщин имеют доброкачественные заболевания МЖ.
Тесная связь патологии МЖ и органов репродуктивной системы объясняется тем, что на функциональное состояние и строение МЖ прямое или косвенное влияние оказывает ряд гормонов через специфические к ним рецепторы: пролактин, саматотропный гормон, стероидные гормоны яичников, гормоны щитовидной железы, коры надпочечников, поджелудочной железы, простагландины и факторы роста.
По данным разных авторов, у 2/3 больных, страдающих ДДМЖ, отмечается абсолютная и относительная гиперэстрогения [2, 8], которая со временем приводит к негативным эффектам: увеличению пролиферации тканей, а также генотоксическому действию эстрогенов, нарушениям процессов деления и гибели клеток, увеличению количества мутаций.
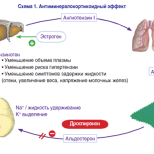
Влияние прогестерона на МЖ может быть как положительным, так и отрицательным (в зависимости от дозы, продолжительности воздействия и от соотношения с эстрогенами). Такое неоднозначное влияние прогестерона на ткани МЖ также связано с его воздействием на различные типы рецепторов – А и В, которые обладают разной функциональной активностью. При этом важное значение имеет соотношение к прогестерону этих двух типов рецепторов – их разное соотношение обуславливает разные эффекты в отношении экзогенного и эндогенного прогестерона.
По этой же причине в последние годы пересмотрен патогенез миомы матки (прогестероновая теория), т.е. причиной роста узлов считают системную или локальную гиперпрогестеронемию при количественном нарушении прогестероновых рецепторов типов А и В. Новые взгляды на некоторые звенья патогенеза миом привели к совершенно другим подходам в лечении данной патологии – применению комбинированных оральных контрацептивов (КОК), агонистов гонадотропных рилизинг-гормонов, а не препаратов прогестеронового ряда.
Таким образом, эстрогены вызывают пролиферацию протокового альвеолярного эпителия и стромы, в то время как прогестерон, противодействуя этим процессам, обеспечивает дифференцировку эпителия и прекращение митотической активности [3, 10].
В связи с вышеизложенным знание сложных механизмов структурно-функционального развития МЖ и методов диагностики его нарушений является чрезвычайно важным для определения терапевтических подходов к лечению ДДМЖ. Терапия ДДМЖ традиционно предполагает применение средств, нормализующих нейропсихический статус, улучшающих функцию паренхиматозных органов, адаптогенов, витаминов, ферментов, неспецифических противовоспалительных средств, препаратов йода. В последние годы широкое распространение получили различные гомеопатические средства, фитотерапия [11]. Безусловно, назначение перечисленных препаратов является обоснованным и направлено на различные звенья процесса формирования патологических изменений в ткани МЖ. Однако, учитывая выраженную гормональную зависимость ткани МЖ, патогенетической терапией ДДМЖ является гормональная коррекция нарушений в гипоталамо-гипофизарно-яичниковой системе.
Вместе с тем следует отметить, что назначение гормональных средств требует тщательного предварительного обследования пациенток и правильного подбора препаратов, поскольку при неудачном выборе терапии может наблюдаться обострение болевого синдрома, пролиферация тканей МЖ, вплоть до развития узловых образований, возникновения кист и т.д.
В последние годы при лечении ДДМЖ используют препараты «центрального действия», т.е. способные в разной степени блокировать выработку гормонов гипоталамо-гипофизарно-яичниковой системы. Местное применение гормонов в данной статье мы не рассматриваем, так как лечение в этом случае является симптоматическим, и его следует назначать в комплексной терапии индивидуально, с учетом возможных разнонаправленных действий местных форм прогестерона.
Для консервативного лечения мастопатии в последние годы применяют антиэстрогены (тамоксифен, фарестон), однако из-за побочных эффектов и необходимости длительного приема указанные препараты очень редко рекомендуют использовать при доброкачественных процессах МЖ. Ограничением применения антиэстрогенов является их способность вызывать гиперплазию эндометрия. Это делает невозможным прием препаратов при ДДМЖ в сочетании с миомой матки и/или гиперплазией эндометрия.
Учитывая важную роль гиперпролактинемии в патогенезе мастопатии, логичным представляется назначение достинекса и бромокриптина, обладающих свойствами гипоталамического и гипофизарного агониста дофамина [2, 8].
Доказано благоприятное влияние антагонистов гонадотропинов (даназол, неместран) и агонистов рилизинг-гормонов на все формы гиперпластических процессов в МЖ. При их использовании наблюдается снижение активности пролиферативных процессов как железистого, так и фиброзного компонентов на фоне инволюции этих структур [3].
Однако их побочные эффекты, связанные с андрогенной активностью и с сопутствующими анаболическими эффектами, также ограничивают их применение в практической гинекологии.
Таким образом, все вышеперечисленные препараты подавляют функцию гипоталамо-гипофизарной системы и при этом имеют разную переносимость и разный профиль безопасности.
Еще одной группой препаратов, которая способна подавлять выработку гормонов в гипоталамо-гипофизарной системе, являются КОК.
История их использования берет свое начало с 1960 г., когда G. Pincus доказал, что применение эстроген-гестагенных препаратов подавляет овуляцию у 100% женщин [16]. Позже были выявлены лечебные свойства КОК при гиперпластических процессах МЖ. Многие исследователи сходятся во мнении о протективном действии этих препаратов в отношении доброкачественных заболеваний и рака МЖ (РМЖ) [6, 11].
При длительном применении низкодозированных КОК частота ДДМЖ снижается на 40%, что связано с обеспечением функционального покоя основных структур МЖ [3, 10]. Лечебное воздействие препаратов выражается в уменьшении и исчезновении симптомов масталгии в течение первых месяцев применения, при этом наблюдается прогрессивное снижение частоты (40%) мастопатии. При назначении КОК иногда появляются или усиливаются уже имеющиеся масталгия и нагрубание МЖ, что ограничивает применение этих препаратов. Однако эти нежелательные явления возникают у небольшого количества женщин, имеют функциональный характер и проходят самостоятельно. Указанные эффекты, согласно множественным литературным данным, не связаны ни с эстрогенным, ни с гестагенным компонентом, они могут возникать на фоне любого режима применения (21 + 7, 24 + 4, 63 + 7), что и отмечено в инструкциях к препаратам. По нашему мнению, появление этих симптомов связано с периодом адаптации, т.е. с периодом, когда меняется исходный уровень гормонов у женщины до уровня гормонов, обусловленных действием КОК. Именно в период снижения уровней гормонов и появляются симптомы. После стабилизации концентрации гормонов симптомы исчезают самостоятельно. Этот процесс является сугубо индивидуальным. Однако масталгия и нагрубание МЖ на фоне КОК могут быть связаны с реакцией прогестероновых рецепторов. Локальная гиперпрогестеронемия приводит к нарушению венозного оттока и к последующему венозному стазу. В результате этого возникает отек стромы МЖ и появляются характерные симптомы, которые проходят самостоятельно, как указывалось выше, или после применения венотоников, верошпирона, мастодинона (Подзолкова Н.М., 2004).
Другой вопрос, который необходимо обсудить, касается РМЖ. Публикации в литературе о возможной связи КОК и РМЖ привели к необоснованным страхам их применения при ДДМЖ. Согласно данным международных исследований, не существует четких доказательств того, что использование КОК повышает риск РМЖ. В некоторых исследованиях указывается на несущественную связь приема КОК и последующего развития РМЖ, однако из-за неоднородности исследований, их генетических и экологических отличий эти исследования нельзя считать достоверными.
ВОЗ подтвердила это. Так, согласно Критериям преемственности (Женева, 2004), КОК имеют критерий безопасности I (безопасны, не имеют ограничений с целью контрацепции при ДДМЖ).
Целью нашей работы явилось изучение исходных особенностей гормонального статуса, уровня факторов роста у женщин репродуктивного возраста с гинекологической патологией (гиперплазией эндометрия, эндометриозом, кистой яичника, фибромиомой матки) и диспластическими заболеваниями МЖ; влияния терапии КОК (Линдинет 20, Новинет) в пролонгированном режиме (непрерывно 3 мес) на гормональные, клинические характеристики и на эффективность профилактики развития рецидивов гиперпластических процессов МЖ и гениталий. Также изучалась эффективность индивидуального подбора КОК (на примере Линдинета 20, Новинета) в пролонгированном режиме (непрерывно 3 мес) в лечении ДДМЖ в зависимости от вида прогестинов и сопутствующей гинекологической патологии.
Материалы и методы
Для решения поставленной задачи были обследованы 300 женщин. 250 из них составляли основную группу: 150 пациенток с ДДМЖ на фоне гинекологической патологии (первая группа), 100 – с гинекологическими заболеваниями без патологии МЖ (вторая группа).
В контрольную группу входили 50 женщин без гинекологической патологии и заболеваний МЖ. Средний возраст обследованных основной группы – 35,97 ± 0,77 года, контрольной – 34,28 ± 0,67 года. Женщины первой и второй групп получали терапию КОК (Линдинет 20, Новинет) в пролонгированном режиме (непрерывно 3 мес) в зависимости от выявленной гинекологической патологии.
Анамнез пациенток изучали по разработанной нами анкете-опроснику. Особое внимание уделяли перенесенным экстрагенитальным заболеваниям, наследственности (гинекологическим, маммологическим и онкологическим заболеваниям у ближайших родственников).
Также была выполнена выкопировка информации из первичной медицинской документации обследуемых в женских консультациях, областном онкологическом диспансере, что позволило корригировать данные опроса. По показаниям было выполнено вагинальное УЗИ с диагностическим выскабливанием цервикального канала и полости матки. Все женщины были осмотрены терапевтом. Также проведено лабораторное обследование – определены уровни таких гормонов, как прогестерон, эстрадиол, пролактин, тестостерон, дегидроэпиандростерон-сульфат, тиреотропный гормон, трийодтиронин, тироксин, онкомаркер МЖ, а также уровни факторов роста. Всем женщинам было выполнено комплексное обследование МЖ, соска и ареолы, регионарных лимфатических узлов (осмотр и пальпация, ультразвуковое сканирование, допплерография, цитологическое исследование выделений из сосков). Всем пациенткам старше 40 лет была проведена маммография.
Результаты исследования и их обсуждение
В последнее время актуальным становится назначение КОК в пролонгированном режиме при различных дисгормональных заболеваниях. Это объясняется тем, что такой режим дает дополнительные преимущества – более стабильные концентрации гормонов в крови по сравнению с циклическим режимом, которые позволяют предотвратить десинхронизацию гипоталамогипофизарной системы, а следовательно более эффективно корректировать гормональные расстройства.
Поэтому представляется интересным изучение клинической эффективности пролонгированного режима применения КОК у пациенток репродуктивного возраста с учетом динамики показателей гормонального статуса и факторов роста.
Изучая профиль безопасности разных групп препаратов, нас заинтересовало применение КОК (Новинета и Линдинета 20) при сочетании ДДМЖ и гинекологической патологии. Это было связано со следующими факторами:
• существуют исследования и публикации об эффективности применения Линдинета 20 при ДДМЖ, однако в достаточной мере не освещен вопрос о гормональной терапии мастопатии в сочетании с гиперпластическими процессами эндометрия, генитальным эндометриозом, миомой матки и эндокринными нарушениями менструально-репродуктивной функции;
• так как при ДДМЖ наблюдается гиперэстрогения, были выбраны два препарата, содержащие минимальное количество этинилэстрадиола (20 мкг);
• поскольку прослеживаются разные морфологические изменения в МЖ при сочетании ДДМЖ с гиперпластическими процессами, эндометриозом (преобладание железистого компоненета и пролиферации), с гиперандрогенией и миомой (преобладание фиброза и кистозных изменений), нами были выбраны препараты с разными прогестинами. Новинет содержит дезогестрел, Линдинет 20 – гестоден.
Разные индексы селективности и способность дезогестрела блокировать оба вида прогестероновых рецепторов (А и В) позволяет подобрать для лечения эти препараты индивидуально. Накоплен достаточный опыт применения Новинета при миомах малых размеров, поэтому нам было интересно провести анализ эффективности использования Новинета при ДДМЖ в сочетании с миомой матки и/или гиперпластическими процессами, при ДДМЖ и гиперандрогенных состояниях (синдроме поликистоза яичников, бесплодии). По этому же принципу назначали Линдинет 20 при ДДМЖ и эндометриозе.
В сравнении с другими прогестагенами третьего поколения гестоден по своей химической структуре наиболее близок к натуральному прогестерону. Кроме того, гестоден обладает выраженными антиэстрогенными свойствами, что помогает нейтрализовать нежелательные метаболические эффекты эстрогенов.
По данным ряда авторов (Colletta A.A. et al., 1991;
Асецкая И.Л., Белоусов Ю.Б., 2001), стимуляция эстрогеновых рецепторов рассматривается как фактор риска развития РМЖ. Выраженное антиэстрогеновое свойство подтверждает целесообразность применения Линдинета 20 при ДДМЖ. В отличие от других гестагенов третьего поколения гестоден не подвергается метаболизму при первичном прохождении через печень, и его биодоступность составляет 100%.
Имеются также данные о способности гестодена дозозависимым способом тормозить рост клеток РМЖ человека, однако для дальнейшего изучения этого вопроса необходимо проведение дополнительных клинических испытаний.
При исследовании гормонального статуса и уровня факторов роста отмечено прямую коррелятивную зависимость (r = +0,83 ± 0,4 р < 0,05) между уровнем эстрадиола в сыворотке крови женщин основной группы и уровнями факторов роста (эпидермальным фактором [ЭФР] роста и фактором роста фибробластов [ФРФ]) и обратная коррелятивная зависимость (r = –0,74 ± 0,6 р < 0,05) между уровнем факторов роста и уровнем прогестерона до начала лечения.
Учитывая тесную взаимосвязь стероидных гормонов между собой, нами также было изучено их соотношение. Мы отметили несоответствие в соотношении прогестерон/эстрадиол до лечения. Если у пациенток основной группы это соотношение в первой и второй группах достоверно не отличалось (2,5 ± 0,05 и 2,9 ± 0,04 соответственно), то в контрольной группе оно было больше в 2,7-3,4 раза и равнялось 8,7 ± 0,02, что указывало на гормональный дисбаланс.
У женщин основной группы до лечения имелись нарушения продукции факторов роста, которые характеризовались достоверно более высокими (в 1,3-2,8 раза большими, чем в контрольной группе) уровнями показателей (р < 0,05).
Также мы отметили изменение в соотношении факторов роста. Так, в группе контроля соотношение трансформирующего фактора роста (ТФР) к ФРФ было больше 2, а соотношение ТФР к ЭРФ больше 4.
У женщин основной группы отмечался дисбаланс уровней исследуемых факторов роста. Так соотношение ТФР/ФРФ было меньше 2, а соотношение ТФР/ЭРФ меньше 4 (р < 0,05).
В основной группе продукция факторов роста характеризовалась снижением их уровня через 3 мес после непрерывного приема КОК: ТФР с 586,3 ± 15,9 пкг/мл до 126,2 ± 12,2 пкг/мл; ЭФР с 106,7 ± 16,9 пкг/мл до 30,2 ± 0,2 пкг/мл; ФРФ с 232,2 ± 11,2 пкг/мл до 56,7 ± 1,3 пкг/мл. У пациенток, которые получали назначенное нами лечение, мы отметили достоверное снижение уровня факторов роста, и через 3 мес применения КОК они соответствовали уровням женщин контрольной группы.
Всего 2% пациенток отметили межменструальные кровянистые выделения в первые два месяца приема КОК, которые прекратились на третьем месяце приема.
Явления мастодинии на фоне приема КОК были выражены у 4% лиц основной и 6% – контрольной групп в течение первого месяца приема препарата, которые затем проходили самостоятельно.
За время наблюдения ни у одной больной не выявлено перехода диффузной формы мастопатии в узловую;
большинство пациенток отметили исчезновение симптомов, характерных для мастодинии (резкое нагрубание МЖ, болезненность перед менструациями).
Нормализация гормональных показателей на фоне дифференцированного применения КОК (Линдинет 20, Новинет) в зависимости от сопутствующей гинекологической патологии коррелировала с результатами оценки уровней факторов роста. У 92% пациенток на фоне использования КОК была отмечена нормализация соотношения уровней исследуемых гормонов и факторов роста, значительное уменьшение клинических проявлений мастопатии.
Таким образом, применение КОК не противопоказано больным ДДМЖ. При лечении диффузной мастопатии в сочетании с гинекологической патологией в качестве метода выбора можно рекомендовать использование в непрерывном режиме монофазных гормональных препаратов, содержащих прогестагены третьего поколения – гестоден (Линдинет 20) и дезогестрел (Новинет).
Выводы
1. Поскольку при сочетании ДДМЖ с гиперпластическими процессами гениталий прослеживаются различные морфологические изменения в МЖ, нами были выбраны препараты с разными прогестинами.
При ДДМЖ в сочетании с миомой матки и/или гиперпластическими процессами, при ДДМЖ и гиперандрогенных состояниях (синдроме поликистоза яичников, бесплодии) назначали Новинет; при ДДМЖ и эндометриозе – Линдинет 20.
2. У женщин основной группы отмечался дисбаланс уровней исследуемых факторов роста. Так, до лечения соотношение ТФР/ФРФ было меньше 2, соотношение ТФР/ЭРФ – меньше 4 (р < 0,05). У пациенток, которые получали назначенное нами лечение, отмечалось достоверное снижение уровней факторов роста, а через 3 мес непрерывного применения КОК их уровни соответствовали таковым женщинам контрольной группы.
3. За время наблюдения ни у одной больной не выявлено перехода диффузной формы мастопатии в узловую; большинство из них отметили исчезновение симптомов, характерных для мастодинии.






Отзывов нет
Комментариев пока нет.
Оставьте свой отзыв